
立即掃碼咨詢
聯系方式:400-822-6768
聯系我們時請說明在儀器網(www.189-cn.com)上看到的!
1. 引言
蝦青素來源有兩種,天然提取和人工合成 [1] [2]。目前天然蝦青素的來源中,以微藻的前景Z為廣闊,特別是雨生紅球藻。雨生紅球藻中的蝦青素以其高活性及高含量,成為近年來的研究熱點。蝦青素也廣泛存在于生物界,特別在蝦、蟹、魚體內含量較高,是海洋生物體內主要的類胡蘿卜素之一。另外,一些藻類也能產生蝦青素,例如雨生紅球藻、綠球藻等微藻及海帶等大型海藻中都有蝦青素的分布。蝦青素的化學名為3,3’-二羥基-β,β’-胡蘿卜素-4,4’-二酮,分子式C40H52O4,相對分子質量596.86,是一種萜烯類不飽和化合物,其化學結構由4個異戊二烯單位以共軛雙鍵的形式連接,在其兩端2個烯酮單位組成的六元環結構,和β-胡蘿卜素的結構相似,其結構式如下圖1所示。

Figure 1. The structure of astaxanthin
圖1. 蝦青素的結構
2. 蝦青素用途
在食品領域中,蝦青素可以用于飲料、食品、調料的著色,還可以有效地起保鮮作用。
在化妝品領域中蝦青素更是因其抗氧化功效被廣泛應用,蝦青素有著強大的抗氧化作用,可用于對皮膚的保護。因能夠減弱活性氧(ROS)和基質金屬蛋白酶(NMP)對真pi層膠原蛋白和彈力蛋白的破壞,保證了皮膚的正常代謝,從而使得紫外線損傷的皮膚快速得以修復。
在醫療方面,有研究證實蝦青素可以緩解疲勞、增強免疫力、抗炎抗感染等,也可以用于心腦血管疾病的預防甚至抑制腫瘤的形成 [3] [4]。
目前蝦青素已經有商品化的產品,大部分用于化妝品領域。蝦青素具有抗氧化作用,可對皮膚起到一定保護,防止皺紋的出現及色素沉著的加重,目前市面有蝦青素膠囊,蝦青素片,富含蝦青素的精華液以及蝦青素面膜等,其中蝦青素的含量有4 mg,12 mg不等。
3. 蝦青素的提取工藝
蝦青素廣泛存在于生物界中,一些藻類也能產生蝦青素,例如雨生紅球藻、綠球藻等微藻及海帶等大型海藻中都有蝦青素的分布。目前在天然蝦青素的來源中,以微藻的前景Z為廣闊,特別是雨生紅球藻。由于雨生紅球藻的蝦青素含量Z高可達5%以上,遠高于其他原料,利用雨生紅球藻提取蝦青素,極具大規模工業化生產潛力,目前國內也已經開展了雨生紅球藻的規模化養殖。
雨生紅球藻隸屬綠藻門、團藻目、紅球藻科、紅球藻屬,雨生種。其細胞壁較厚,加大了從中提取蝦青素的難度,采用有機溶劑直接萃取的方式,會大大降低蝦青素的提取率,因此對雨生紅球藻細胞進行有效的破壁處理是蝦青素提取工藝中的關鍵步驟,目前從雨生紅球藻中提取蝦青素分為兩個步驟:破壁和提取。
破壁:雨生紅球藻的厚壁孢子具有堅韌的細胞壁,使得蝦青素直接提取率較低。通常需在提取前需將紅球藻進行破壁處理,且蝦青素屬于熱敏性較高的物質,提取過程中易于分解。目前常用的破壁方法主要有:珠磨法、高壓均質法、冷凍法、勻漿法、超聲波法、凍融法、機械研磨法、液氮冷凍法、酶法和化學法等。但對雨生紅球藻進行破壁處理,極易造成蝦青素的損失,如酸法破壁法,該方法額外在體系中添加了酸作為破壁溶劑,增加了產品分離的難度,且酸液不易于回收利用。有些破壁效果較好,因設備要求較高,不利于放大生產,如高壓均質破壁法,該方法破壁需要經過反復多次處理,耗時較長從而導致有效成分被氧化,此外紅球藻在溶液中極易沉降,導致料液不均勻從而堵塞儀器;超高壓破碎該方法采用100~300 mpa高壓破碎,破壁率超過95%,效果較好但對設備要求較高,不易在規模化生產中應用 [5]。所以找到合適的并可以在生產中規模化應用的破壁方法是實驗成功關鍵之一。
提取:從雨生紅球藻中提取蝦青素主要有以下幾種方法:超臨界CO2萃取法、有機溶劑提取法、高壓均質提取法、油提取法和我們的微波提取法等。采用超臨界CO2萃取技術萃取蝦青素是目前國內外研究的熱點技術,該工藝綠色安全環保,但是該方法對設備要求較高,不易放大生產,該方法和高壓均質提取法常用于實驗室研究,因設備投入成本較高,較難工業化生產;油提取法的提取效果較好,但因油難以除去而降低了蝦青素的含量,品質難以提升;有機溶劑提取法生產成本較低,方法簡便,提取率較高,后期處理方便。因此,有機溶劑萃取法在生產中較為常用 [6]。我們實驗室正在應用北京祥鵠微波和超聲波化學儀器改進蝦青素的提取工藝。
4. 蝦青素的合成
關于蝦青素的主要合成路線,按照合成原料結構式的含碳數可以包括有三條 [7] [8]:一是2C10 + C20 → C40路線,二是2C6 + C10 + 2C9 → C40路線,三是2C15 + C10 → C40路線。第三條路線已經由眾多公司實現了工業化,該路線的綜合策略在于先通過各種途徑反應生成相應的C15磷葉立德,再使用C10二醛發生經典的雙Wittig反應生成C40蝦青素。其中本實驗室采用的是線路三的路線,但是在C15的合成中采用了更為溫和高效的方法,使得合成更為安全。以下針對各個路線作一概述 [4]:
合成路線一 [9]:是由兩分子的甲氧基異戊二烯(1)和C10-二醛二甲基縮醛(2)反應生成C20-二醛二甲基縮醛(4)結構,在與兩分子的C10-二烯醚(5)反應生成蝦青素(7)。反應具體路線如下圖2所示。

Figure 2. The synthesis of astaxanthin
圖2. 蝦青素的合成
該反應Z關鍵的過程為1,5號化合物的合成,根據參考文獻 [9] 得出化合物1的制備過程如下圖3。

Figure 3. The synthesis of compound 1
圖3. 化合物1的合成
化合物5是該方法中制備蝦青素的重要原料,其反應原理如下圖4。

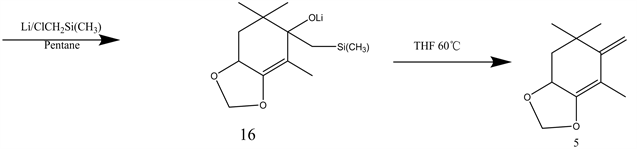
Figure 4. The synthesis of compound 5
圖4. 化合物5的合成
化合物1,5是合成線路一的關鍵原料,正因為其合成的復雜性以及危險性,導致該路線是合成蝦青素的難點之一。
合成路線二 [10]:其具體步驟為以C6醇(17)為原料,生成C6膦鹽(18)后,兩分子的18和C10-二醛(19)反應,生成C22的共軛二炔多烯化合物(20),再與C10-二烯酮(22)反應,經過還原后,生成蝦青素(7)。反應路線如下圖5。

Figure 5. The synthetic route 2 of astaxanthin
圖5. 蝦青素的合成路線二
其中原料8和13是制備蝦青素的關鍵產品,原料8屬于維A醇,但其價格十分昂貴,成為該反應的制備的一大難題。原料13與上述原料5制備基本相似。
合成路線三:
該線路已經在國外的羅氏公司、BASF公司實現了工業化,因此該路線也更適合應用于工業大規模生產。該反應分為兩部分:C9 + C6 = C15和C15 + C10 + C15 = C40。
C9的合成:以氧代異佛爾酮為起始原料,雙鍵在堿性條件下環氧化,堿性水解,氫化還原,羥基和羰基的雙護,得到重要中間體C9合成單元。該路線與上述化合物11合成15路線一致。
C6單元的合成兩公司有著輕微的區別:
羅氏公司C6單元的合成:丙酮和甲醛水溶液在微堿性條件下發生羥醛反應得到羥基丁酮,草酸脫水得到丁烯酮,同乙炔加成,硫酸重排得到重要的中間體六碳醇,此化合物是合成維生素A的重要中間體,將其羥基保護后得到此路線合成蝦青素的C6合成單元。如下圖6。
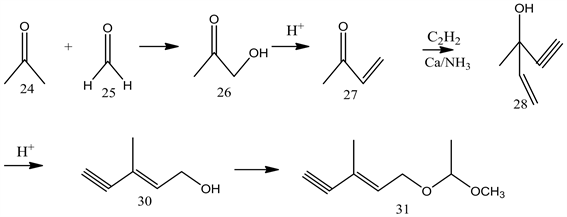
Figure 6. The synthesis of compound 31
圖6. 化合物31的合成
BASF公司前面三步反應同羅氏公司采用的合成工藝路線一樣得到C6叔醇,但生成的叔醇不用酸催化重排轉位,而是將羥基直接保護后去與C9單元反應。其反應路線如下圖7 [8] [11]。

Figure 7. The synthesis of compound 29
圖7. 化合物29的合成
羅氏公司C15單元的合成:C6合成單元的炔基用二異丙氨基鋰處理后與C9合成單元的羰基加成,在酸催化下水解脫保護和叔醇脫水,再選擇炔鍵還原成雙鍵,與三苯基膦溴化氫反應得到C15三苯基鹽 [12] [13] [14],如下圖8。

Figure 8. The synthesis of compound 35
圖8. 化合物35的合成
BASF公司路線對C15合成單元的合成:C6合成單元的炔基與鋰試劑作用形成炔基鋰,與C9合成單元的羰基加成得到C15骨架,水解脫水脫保護,三鍵部分氫化形成雙鍵,得到的叔醇再與三苯基膦溴化氫復合物反應得到C15三苯基膦鹽。如下圖9。

Figure 9. The synthetic route 2 of compound 35
圖9. 化合物35的合成路線二
Z后2分子C15和C10進行經典的Wittig反應合成蝦青素,反應式如下圖10。

Figure 10. The synthetic route 3 of astaxanthin
圖10. 蝦青素的合成路線三
實驗室應用C15 + C10 + C15 = C40的方法,應用的是C13 + C2 = C15。后續的2分子C15和C10進行經典的Wittig反應合成蝦青素跟上述方法一致。該方法合成路線優點是反應較為溫和。其合成路線為 [15] [16]:以α-紫羅蘭酮(43)為起始原料,經過7步反應生成C15三苯基膦(35)結構,再與C10-多烯二醛反應,Z終生成蝦青素(7)。具體路線如下圖11:

Figure 11. Laboratory synthesis of astaxanthin
圖11. 蝦青素的實驗室合成
從反應三條線路中都可以看出2,7,-二甲基-2,4,6-辛三烯-1,8-二醛(19)結構是反應中關鍵的中間體,線路一中的(4)是C10的兩個醛基進行保護,所以需要進行C10結構的合成,現在概述主要的合成路線 [6]。
方法一為BASF公司以1,4-二鹵-2-丁烯(39)為原料,經Abrozov重排反應得到雙磷酸酯化合物,再與丙酮醛縮二甲醇進行Wittig-Horner反應、脫保護基得到十碳三烯雙醛 [17] [18] [19],其反應式如下圖12。

Figure 12. The synthesis of compound 19
圖12. 化合物19的合成
方法二是Hagen以苯亞磺酸鈉為連接劑,與兩分子的2-(3-氯-1-甲基-1-丙烯基)-5,5-二甲基-1,3二噁烷合成砜化合物,再通過強堿消除Z終得到2,7,-二甲基-2,4,6-辛三烯-1,8-二醛 [20]。如下圖13。

Figure 13. The synthetic route 2 of compound 19
圖13. 化合物19的合成路線二
方法三是以呋喃為起始原料,與甲醇經過兩步加成得到1,l,4,4-四甲氧基-2-丁烯,此雙縮醛化合物在路易斯酸催化下與丙烯基甲醚縮合反應得到C10骨架,再經堿處理消除甲醇形成雙鍵得到目標產物。此路線的缺點是丙烯醚原料難得,且化學性質不穩定,與縮醛的加成反應副產物較多 [4]。
5. 蝦青素的生物活性研究
蝦青素是一種含氧的類胡蘿卜素,其分子結構中碳骨架由多聚烯鏈和位于兩側的芳香環組成,同時芳香環上含有羥基和酮基。近年來,國內外大量研究表明,因蝦青素獨特的化學結構,使其具有很強的抗氧化活性,可以預防ai癥、動脈粥樣硬化、糖尿病等慢性病的發展,具有提高免疫力、延緩衰老有積極作用。
蝦青素是一個非常優良的具有抗氧化清除氧自由基功效的化學物質。現已經探明,人體內存在的氧自由基,是百病之源、衰老之魁。這些自由基也被稱為“氧毒”,它們是不成對電子的原子、分子,對人體器官組織和免疫系統具有很強的攻擊能力。如:攻擊細胞膜、脂蛋白、侵蝕胰島細胞、損害關節膜、侵蝕晶狀體和腦細胞、攻擊毛細血管、攻擊人體免疫系統、激發人體釋放因子、攻擊復制中的DNA等。實驗證明,蝦青素在防止亞油酸自氧化、清除羥自由基、清除1,1-二苯代苦肼基(DPPH)的實驗中,都表現出良好的效果。也正因為其化學結構不同于其他類胡蘿卜素,除了有長的共軛雙鍵外,在兩端的芳香環中的羥基和不飽和酮基具有活潑的電子效應,能向自由基提供電子或吸引自由基的未配對電子。達到清除自由基的目的 [21]。
除了強大的抗氧化活性外,蝦青素還具有抗動脈粥樣硬化、抗ai活性和增強免疫功能的活性。研究表明,蝦青素可以升高高密度脂蛋白(HDL),降低低密度脂蛋白(LDL)。對于動脈粥樣硬化有很好的預防作用 [22]。越來越多的研究表明,蝦青素具有抑癌、抗ai作用,這些作用主要體現在蝦青素預防腫瘤的發生、抑制腫瘤細胞增殖、促進腫瘤細胞凋亡、抑制腫瘤轉移、增強免疫、增加細胞間通訊等方面 [23]。另外,有動物實驗發現,蝦青素會增加IL-2的產生,并能促進脂多糖誘導的淋巴細胞的增殖。蝦青素可以增強pizang細胞對抗原的免疫應答,增強抗體的生成 [24] [25],促進免疫細胞的增殖以此來增強免疫功能。
由于蝦青素結構中有兩個手性中心,分別是兩端環結構的C-3和C-3’,兩個手性碳均可以R或S構型存在,所以蝦青素存在光學異構體,分別為3R,3’R,3S,3’S,和內消旋體。不同結構其生物活性會有區別 [26],雨聲紅球藻中的蝦青素均以反式結構存在,并且是3S,3’S的結構,實驗表明,蝦青素無論是清除自由基的能力還是提高免疫活性的能力,其內消旋結構活性都是Z差的。所以純化蝦青素也是提高其生物活性的一大優勢。
6. 小結與展望
越來越多的實驗表明蝦青素具有強大的抗氧化能力,其強抗氧化能力已經逐漸進入到食用色素、畜牧業和水產品的飼料添加劑中,也廣泛應用于化妝品、保健品和醫藥等行業中 [27]。當然,蝦青素的抗氧化機制及作用為預防和治療腫瘤、心血管疾病及各種慢性疾病提供了理論基礎。雖然關于蝦青素研究已經取得了很大的進展,但未來我們仍需要不斷的實驗研究,找到更安全的簡便的方法來提取和合成蝦青素,我們實驗室正在應用祥鵠微波化學系列儀器改進蝦青素的萃取方法和合成路線 [28] [29],為進一步研究蝦青素的生物活性、構效關系及其工業化提供基礎。
NOTES
*通訊作者。
參考文獻
| [1] | 李元廣, 章真, 等. 一種利用微藻高效生產蝦青素的方法[P]. 中國專利, CN103571906A. 2014. |
| [2] | 李悅明, 管松, 等. 一種從雨生紅球藻中提取蝦青素的方法[P]. 中國專利, CN103787941A. 2014. |
| [3] | 解溫品, 秦士新. 自由基醫學研究進展[J]. 中華損傷與修復雜志, 2012, 7(2): 194-195. |
| [4] | 李勇, 孔令青, 等. 自由基與疾病研究進展[J]. 動物醫學進展, 2008, 29(4): 85-87. |
| [5] | 許晟, 陳可泉, 等. 一種雨生紅球藻細胞快速破壁偶聯萃取蝦青素的方法[P]. 中國專利, CN106748944A. 2017. |
| [6] | 楊枝中, 萬近福, 等. 一種從雨生紅球藻中提取蝦青素(油)的方法[P]. 中國專利, CN108440359A. 2018. |
| [7] | George, S., Schloemer, C.A., et al. (2002) Preparation of 4,4’-Diketo-Beta, Beta-Carotene Derivaives. US, 6372946. |
| [8] | Widmer, E., Zell, R., Broger, E.A., et al. (1981) Technical Procedures for the Synthesis of Carotenoids and Related Compound from 6-Oxo-Isophorone. Helvetica Chimica Acta, 64, 2419-2446. |
| [9] | Rüttimann,
A. (1999) Dienolether Condensations—A Powerful Tool in Carotenoid
Synthesis. Pure and Applied Chemistry, 71, 2285-2293. https://doi.org/10.1351/pac199971122285 |
| [10] | 陳志榮, 李浩然, 王純超, 等. 一種蝦青素的合成方法[P]. 中國專利, CN1260211C.2004. |
| [11] | Bernd, R., Petra, D., Thomas, M., et al. (2006) Method for Producing Astaxanthin and Canthaxanthin Intermediate Products: WO. |
| [12] | Ernst, H. 蝦青素的制備, 制備它的新中間體以及其制備[P]. 中國專利, ZL94108274.1. |
| [13] | Ernst, H., Paust, J., et al. (1993) Preparation of Canthaxanthin and Astaxanthin. US5210314. |
| [14] | Krause, W., Henrich, K., Paust, J., et al. (1997) Preparation of Astaxanthin. |
| [15] | 皮士卿, 陳新志, 胡四平, 等. 蝦青素的合成[J]. 有機化學, 2007, 27(9): 1126-1128. |
| [16] | 皮士卿. 類胡蘿卜素合成工藝研究[D]: [博士學位論文]. 杭州: 浙江大學, 2008. |
| [17] | 田金金, 呂國鋒, 管敏蝦, 等. 一種蝦青素中間體的合成方法[P]. 中國專利, CN10911883. 5. 2018. |
| [18] | Babler, J.H. (1992) Method of Making 2,7-Dimethyl-2,4,6-octatrienedial and Derivatives Thereof. US, 5107030A. |
| [19] | Bemhard, K. and Mayer, H. (1991) Recent Advances in the Synthesis of Achiral Carotenoids. Pure and Applied Chemistry, 63, 35-44. https://doi.org/10.1351/pac199163010035 |
| [20] | Jaedicke, H., Kaiser, K. and Amm, H.M. (1993) Process for the Preparation of Polyenes via Julia Reaction in Ketone and Other Solvents. EP, 523534A2. |
| [21] | 陳晉明, 王世平, 馬儷珍, 等. 蝦青素抗氧化活性研究[J]. 營養學報, 2007(2): 163-165, 169. |
| [22] | Murillo, E. (1992) Hypercholesterolemic Effect of Canthaxanthin and Astaxanthin in Rats. Archivos Latinoamericanos De Nutrición, 42, 409. |
| [23] | 呂亭亭, 葛聲. 蝦青素抗腫瘤作用的研究進展[J]. 腫瘤代謝與營養電子雜志, 2015(4): 58-62. |
| [24] | Jyonouchi, H., et al. (1995) Astaxanthin, a Carotenoid without Vita-Min a Activity, Augments Antibody Responses in Cultures Including T-Helper Cell Clones and Suboptimal Doses of Antigen. Journal of Nutrition, 125, 2483-2492. |
| [25] | Jyonouchi,
H., Sun, S., Mizokami, M. and Gross, M.D. (1996) Effects of Various
Carotenoids on Cloned, Effector-Stage T-Helper Cell Activity. Nutrition
and Cancer, 26, 313-324. https://doi.org/10.1080/01635589609514487 |
| [26] | 孫偉紅. 不同來源蝦青素的分離制備及其構效關系研究[D]: [博士學位論文]. 青島: 中國海洋大學, 2015. |
| [27] | 江利華, 柳慧芳, 郝光飛, 等. 蝦青素抗氧化能力研究進展[J]. 食品工業科技, 2019, 10(40): 350-354, 195. |
| [28] | 胡曌璽, 王存文, 閔清, 尤進茂, 馬密霞, 胡文祥. 微波化學研究進展——京東祥鵠微波化學聯合實驗室微波化學領域相關研究成果目錄及部分論文集[M]. 武漢: 漢斯出版社, 2019. |
| [29] | 秦寧, 閔清, 馬密霞, 胡文祥. 微波輔助提取中藥成分研究進展[J]. 微波化學, 2018, 2(3): 79-84. https://www.hanspub.org/journal/PaperInformation.aspx?paperID=27557 |
相關產品
全部評論(0條)
推薦方案
相關解決方案
參與評論
登錄后參與評論